Intransparenz auf Kassenkosten
Mit einer neuen „Pharmastrategie“ will die Bundesregierung Deutschland zum führenden Standort für Entwicklung und Produktion von Arzneimitteln machen. Die Krankenkassen fürchten, dass die Ampel auf Kosten der Beitragszahler die Transparenz bei der Preisbildung für Medikamente opfert.
Noch ist es nur ein Aktionsplan. Die vom Bundeskabinett im Dezember 2023 verabschiedete „Pharmastrategie“ umfasst drei Bereiche: Zum einen will die Ampel-Koalition bessere Rahmenbedingungen für Arzneimittelforschung und -produktion schaffen. Zum zweiten geht es um eine beschleunigte Digitalisierung des Gesundheitswesens. Zudem will der Bund innovative Projekte der Pharmaindustrie fördern. Bundesgesundheitsminister Karl Lauterbach (SPD) sprach nach dem Kabinettsbeschluss von schnelleren Zulassungsverfahren, unbürokratischen Genehmigungen und der Vereinfachung von Ethik-, Strahlenschutz- und Datensicherheitsprüfungen. Die Regierung verspricht der Industrie zudem weitere finanzielle Förderung – unter anderem für neue Produktionsstätten und Forschung an knappen Medikamenten wie Antibiotika. Verantwortlich für die notwendige konkrete gesetzliche Umsetzung wären neben Lauterbach auch Wirtschaftsminister Robert Habeck (Grüne) und Forschungsministerin Bettina Stark-Watzinger (FDP).
Die Weichen für das Konzept wurden auf einem „Pharmagipfel“ Ende November in Berlin gestellt. Entsprechend positiv bewerteten die Industrieverbände das Ampel-Paket. „Die Pharmastrategie ist eine große Chance für den Standort Deutschland“, lobte Han Steutel, Präsident des Verbandes der forschenden Pharmaunternehmen, das Vorhaben. Hubertus Cranz, Hauptgeschäftsführer des Bundesverbandes der Arzneimittel-Hersteller (BAH), betonte, dass eine Wertschätzung der Arzneimittel-Hersteller als Leitindustrie „lange vermisst“ worden sei. Vertreter der gesetzlichen Krankenversicherung (GKV) waren zum Pharmagipfel nicht geladen. Der AOK-Bundesverband hatte deshalb schon im Vorfeld vor „vermeintlichen Lösungen zulasten der Beitragszahler“ gewarnt.
Aus Sicht der GKV hat sich diese Befürchtung bewahrheitet. Denn die Bundesregierung hat eine Kernforderung der Pharmaunternehmen übernommen. Im Strategiepapier heißt es: „Die Ablösung des öffentlich gelisteten Erstattungsbetrags durch einen vertraulichen Erstattungsbetrag im Rahmen der Erstattungsbetragsverhandlungen wird ermöglicht.“ Weniger formal ausgedrückt: Künftig soll vertraulich bleiben, welche Rabatte die Pharmaunternehmen den Krankenkassen und anderen Kostenträgern auf die von den Herstellern weiterhin selbst bestimmten Preise einräumen.
Weiterer Anstieg der Arzneiausgaben droht

Die Krankenkassen lehnen das vehement ab. „Das würde zu noch mehr Intransparenz bei der Preisbildung und zur Anhebung des ohnehin hohen Preisniveaus führen und die Arzneimittelpreise in Deutschland weiter hochschaukeln“, erläutert der stellvertretende Vorstandsvorsitzende des AOK-Bundesverbandes, Jens Martin Hoyer. Die AOK-Gemeinschaft unterstütze das Ziel der Bundesregierung, die Rahmenbedingungen für den Forschungs- und Produktionsstandort Deutschland zu verbessern. Es brauche eine zuverlässige Arzneimittelversorgung mit verlässlichen, nachvollziehbaren und einfach umsetzbaren Rahmenbedingungen für die Preisbildung und Kostenerstattung durch die Krankenkassen. „Die GKV-Finanzstabilität dürfen wir dabei aber nicht aus dem Blick verlieren“, so der Verbandsvize.
Unmittelbarer Marktzugang als Vorteil
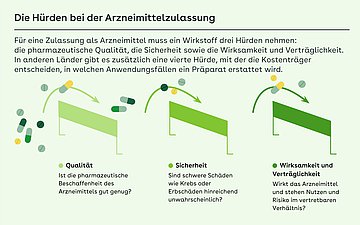
Die Arzneimittelversorgung in Deutschland ist nicht nur durch öffentlich gelistete und damit transparente Preise gekennzeichnet, sondern auch durch den in Europa einzigartigen unmittelbaren Marktzugang neuer Arzneimittel für die Versorgung der Versicherten. Eine Angleichung der bestehenden Rahmenbedingungen an die Praxis in anderen europäischen Ländern, die neben vertraulichen Rabatten üblicherweise ergänzend auch eine Auswahl treffen, ob und in welchem Umfang sie die Präparate erstatten, wäre mit umfangreichen Voraussetzungen verbunden.
Die Bundesregierung will zwar sicherstellen, „dass vertrauliche Erstattungsbeträge bei neuen Arzneimitteln nicht zu Mehrausgaben oder zu neuer Bürokratie für das deutsche Gesundheitswesen führen“. Diese Zielvorgabe dürfte aber nicht zu halten sein. Auch wenn die Umsetzung derzeit noch unklar ist – notwendige Folgeregelungen dürften in jedem Fall zu mehr bürokratischem Aufwand führen. Denn wenn die Rabatte nicht mehr öffentlich wären, müssten die Pharmaunternehmen künftig allen „Anspruchsberechtigten“ einzeln mitteilen, welchen Rabatt sie mit dem GKV-Spitzenverband als zentralem Verhandlungspartner ausgehandelt haben. Die Differenz zum eigenen Markteinstiegspreis müssten sie den „Anspruchsberechtigten“ dann erstatten. Das wären neben den gesetzlichen Krankenkassen, den privaten Krankenversicherungen und den Krankenhäusern auch die Beamten-Beihilfe des Bundes und der Länder sowie die Justizvollzugsanstalten. Zudem müssten die vertraulichen Rabatte bei weiteren Erstattungsverhandlungen im Gesundheitswesen berücksichtigt werden, insbesondere bei Verhandlungen zwischen GKV-Spitzenverband und Apotheken über die sogenannte Hilfstaxe. Dabei geht es um die Preisbildung von Rezepturen, die in einer Apotheke hergestellt werden.
Sollten vertrauliche Rabatte zu Wettbewerbsprodukten künftig bei Erstattungsbetragsverhandlungen nicht mehr berücksichtigt werden, müsste das gesetzliche Verfahren zur Nutzenbewertung und Preisbildung bei neuen Medikamenten (AMNOG), bei dem die Preise der zweckmäßigen Vergleichstherapie wie auch der vergleichbaren Arzneimittel herangezogen werden, gravierend umgebaut werden. Das Verfahren müsste folglich durch eine neue Systematik ersetzt werden.
Ergänzend sind erhebliche Mehrausgaben infolge einer Vertraulichkeit des Erstattungsbetrags absehbar: Das zu erwartende immer weiter fortschreitende Auseinanderklaffen von Listenpreisen und tatsächlichen Abgabepreisen für immer größere Teile des Marktes ließe den Umfang der Rückabwicklungen mit der Zeit deutlich steigen. Die damit verbundene Vorfinanzierung überhöhter Preise durch die GKV würde die Liquidität der Krankenkassen erheblich belasten – und dies bei inzwischen erheblich geschrumpften Rücklagen. Zahlungsverzögerungen oder gar Ausfälle bei den Rückzahlungen durch die Pharmaunternehmen träfen die Solidargemeinschaft unmittelbar und müssten kompensiert werden. Immer höhere Vorleistungen und Liquiditätsrisiken der Kassen wären letztlich beitragssatzrelevant.
AMNOG-Verfahren
Für insgesamt 395 Arzneimittel sind seit 2011 Erstattungsbeträge zwischen dem jeweiligen Pharmahersteller und dem GKV-Spitzenverband vereinbart oder von der Schiedsstelle festgesetzt worden. In dieser Übersicht des GKV-Spitzenverbandes sind auch jene Arzneimittel enthalten, die ein Pharmaunternehmen aus dem Verkehr genommen hat.
Quelle: GKV-Spitzenverband
Zudem ist zu berücksichtigen, dass mit ausbleibender Korrektur des vom pharmazeutischen Unternehmen selbst gewählten Preises durch den ausgehandelten Erstattungsbetrag das Preisniveau noch deutlich stärker steigt, als dies bereits jetzt beklagt wird. Nicht umsonst hat die Bundesregierung das AMNOG im Jahr 2022 durch das GKV-Finanzstabilisierungsgesetz angepasst, um das bestehende überhöhte Preisniveau der bis dahin verhandelten Erstattungsbeträge zu korrigieren.
Eine Schwächung dieser Korrekturmechanismen durch die Einführung der Vertraulichkeit dürfte dazu führen, dass steigende offizielle Listenpreise als Preisanker für Nachfolgeprodukte in immer höhere Rabatte münden.
Ebenso würde der wünschenswerte Wettbewerb durch Zweitanbieter oder Importeure und Wettbewerber im gleichen Anwendungsgebiet durch eine solche Maßnahme sehr stark gehemmt. Wenn es keine Preistransparenz mehr gibt, fehlt ein essenzieller Bezugspunkt für die Feststellung von Preisgünstigkeit und Wirtschaftlichkeit. Entsprechend könnten Effizienzreserven weder bei der Preisbildung der Arzneimittel selbst noch im Verordnungsgeschehen durch ärztliche Praxen und Krankenhäuser erschlossen werden.
Preistransparenz stärkt Wettbewerb
Die von der Pharmaindustrie angestrebte Intransparenz dürfte sich letztlich außerdem auf den Generikamarkt auswirken. Denn das Verhindern jeglicher direkter Preiskonkurrenz während der Patentphase würde den Wettbewerb nach Patentablauf verzögern. So wird letztlich auch die Neubildung von wirtschaftlichen Arzneimittel-Festbetragsgruppen konterkariert. Transparente Preise leisten darüber hinaus einen wichtigen Beitrag für effektive kartellrechtliche Kontrollmaßnahmen und Interventionen, wie zuletzt bei den durch die EU-Kommission verhängten Millionen-Geldbußen gegen Pharmaunternehmen, die Mindestpreise und Verkaufsquoten für den Arzneimittelwirkstoff Butylscopolamin abgesprochen hatten.
Es verwundert daher wenig, dass durch Vertraulichkeit und Intransparenz gekennzeichnete Preisbildungsinstrumente im Ausland vor allem dadurch erfolgreich sind, dass sie mit einer Auswahlentscheidung durch die Kostenträger verbunden werden: Nicht jedes Produkt, das arzneimittelrechtlich zugelassen ist, wird in anderen Ländern von den Kostenträgern auch erstattet. Nur mit einer solchen sogenannten vierten Hürde – über die für die Zulassung in der EU notwendigen Voraussetzungen bei Qualität, Sicherheit sowie Wirksamkeit/Verträglichkeit hinaus – kann es Krankenversicherungssystemen gelingen, angemessene Erstattungsbeträge durchzusetzen. Wird ein vertraulicher Erstattungsbetrag ohne eine solche Auswahlmöglichkeit implementiert, drohen in Deutschland Mehrausgaben für die Solidargemeinschaft, die nicht mehr zu stemmen sind.
Nutzenbewertung
Alle neuen Arzneimittel unterliegen in Deutschland innerhalb der ersten sechs Monate nach Markteinführung einer Nutzenbewertung durch den Gemeinsamen Bundesausschuss (GBA). Dabei geht es um die Frage, ob das Präparat einen zusätzlichen patientenrelevanten therapeutischen Effekt gegenüber der bisherigen Standardbehandlung für die jeweilige Erkrankung hat. Kriterien sind vor allem längere Lebenszeit, besserer Gesundheitszustand, kürzere Krankheitsdauer, geringere Nebenwirkungen oder bessere Lebensqualität. Basis der Bewertung sind Unterlagen des Pharmaherstellers zum Arzneimittel, die dieser mit Marktzugang des neuen Präparats beim GBA einreicht.
Quelle: Lexikon
Vor dem Hintergrund der benannten Probleme eines vertraulichen Erstattungsbetrages stellt sich die Frage nach der Notwendigkeit einer solchen Maßnahme. Betrachtet man die Marktentwicklung neuer, patentgeschützter Arzneimittel, zeigt sich, dass die Behauptung der Pharmahersteller, die Rahmenbedingungen seien insbesondere für neue Arzneimittel schwierig, nicht nachvollziehbar ist. Deutschland belegt laut der Erhebungen der European Federation of Pharmaceutical Industries (EFPIA), eines europäischen Dachverbandes der nationalen Verbände forschender Pharmaunternehmen, seit Jahren einen Spitzenplatz im internationalen Vergleich bezüglich eines schnellen, umfassenden und qualitativ gesicherten Zugangs zu neuen Arzneimitteln.
Erhalt der Finanzierbarkeit als Ziel

Demnach scheinen die Rahmenbedingungen in Deutschland für die Pharmaseite ein sehr gutes Verhältnis zwischen Innovationsoffenheit und Wirtschaftlichkeit der Arzneimittelversorgung zu schaffen. In den vergangenen zehn Jahren sind deutlich mehr neue Wirkstoffe eingeführt worden als im zeitlichen Umfeld der AMNOG-Einführung und der damit verbundenen Steuerung der Kostenentwicklung zum 1. Januar 2011. Die Nettokosten für den Markt der patentgeschützten Arzneimittel haben sich nahezu verdoppelt. Zugleich haben die Sozialbeiträge bereits die Grenze von 40 Prozent überschritten. Es ist deshalb dringend notwendig, die Bezahlbarkeit des Gesundheitssystems für die Versichertengemeinschaft wieder stärker in den Fokus zu nehmen. Entsprechende Korrekturen für den Patentmarkt hat die Ampel-Koalition mit dem GKV-Finanzstabilisierungsgesetz auf den Weg gebracht. Die damit verbundenen Einsparungen liegen jedoch nach bisherigem Kenntnisstand noch deutlich unter den Erwartungen des Gesetzgebers . Die vorliegenden Reformüberlegungen konterkarieren grundsätzlich das Ansinnen, die Ausgaben insbesondere für Patentarzneimittel finanzierbar zu halten. Dabei ist nicht erkennbar, wie die Mehrkosten aufgrund einer Vertraulichkeit des Erstattungsbetrags das Ziel der Pharmastrategie unterstützen, den Standort Deutschland zu stärken. Denn dass Deutschland als Absatzmarkt insbesondere für Patentarzneimittel eine hohe Attraktivität hat, ist unstrittig. Die Mehrausgaben kommen allen Arzneimittelherstellern zugute, unabhängig von ihrem Produktionsstandort.
Vor diesem Hintergrund sollte die Bundesregierung am transparenten und öffentlich gelisteten Erstattungsbetrag festhalten. Aus Sicht der AOK-Gemeinschaft können andere Maßnahmen zur Förderung der Forschung und Entwicklung von neuen Wirkstoffen in Deutschland einen gezielten und besseren Beitrag leisten, um den Pharmastandort zu stärken. Hierzu zählen die von der Bundesregierung ebenfalls angestrebten besseren Rahmenbedingungen für die Genehmigung und Durchführung von klinischen Studien. Grundsätzlich aber ist die Wirtschaftsförderung für den Pharmastandort Deutschland keine Aufgabe der Beitrag zahlenden Versicherten in der Solidargemeinschaft der GKV, sondern des Staates. Und die muss er mit entsprechenden Mitteln aus dem Bundeshaushalt finanzieren.
Mitwirkende des Beitrags

Autorin

Autor
Datenschutzhinweis
Ihr Beitrag wird vor der Veröffentlichung von der Redaktion auf anstößige Inhalte überprüft. Wir verarbeiten und nutzen Ihren Namen und Ihren Kommentar ausschließlich für die Anzeige Ihres Beitrags. Ihre E-Mail-Adresse wird nicht veröffentlicht, sondern lediglich für eventuelle Rückfragen an Sie im Rahmen der Freischaltung Ihres Kommentars verwendet. Die E-Mail-Adresse wird nach 60 Tagen gelöscht und maximal vier Wochen später aus dem Backup entfernt.
Allgemeine Informationen zur Datenverarbeitung und zu Ihren Betroffenenrechten und Beschwerdemöglichkeiten finden Sie unter https://www.aok.de/pp/datenschutzrechte. Bei Fragen wenden Sie sich an den AOK-Bundesverband, Rosenthaler Str. 31, 10178 Berlin oder an unseren Datenschutzbeauftragten über das Kontaktformular.



1 Kommentar
Markus
Transparenz ist ein wichtiges Merkmal von Demokratie.
Transparenz ist eine Voraussetzung für Mündigkeit und Selbstwirksamkeit.
Im Gesundheitswesen ist Transparenz eine Voraussetzung für Vertrauen.